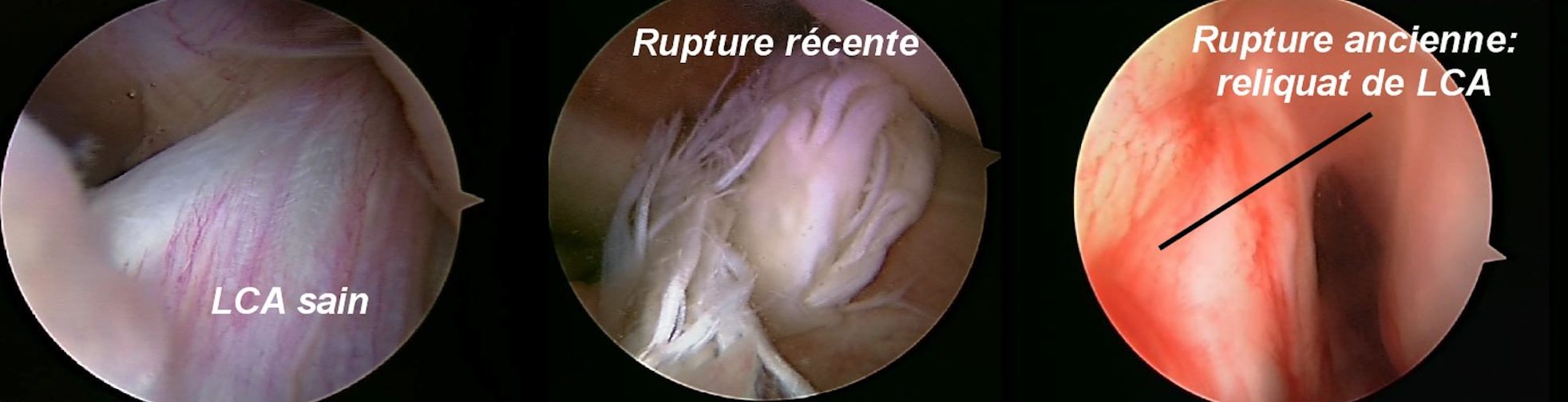
Qu’est-ce qu’une entorse grave du genou par rupture du ligament croisé antérieur (LCA) ?
Les lésions ligamentaires du genou ont vu leur fréquence accroître au cours de ces 20 dernières années parallèlement au développement de la pratique sportive « grand public ». Elles sont consécutives à des mécanismes d’entorse, situations dans lesquelles les tissus (capsule articulaire, ligaments, muscles et/ou tendons) du genou dépassent leur limite élastique et se déchirent.
Tous les stades de gravité des entorses peuvent être observés, depuis l’entorse bénigne du ligament latéral interne (LLI) jusqu’à la luxation du genou. Entre ces deux extrêmes, l’entorse grave avec rupture complète du ligament croisé antérieur (LCA) est particulièrement fréquente puisqu’on évalue le risque de sa survenue à 1/3000. A titre d’exemple, 200000 reconstructions ligamentaires pratiquées aux U.S.A chaque année. Ce problème est devenu un enjeu de santé publique et justifie donc des mesures de prévention (bon réglage des fixations de ski par exemple).
Comment se fait on une entorse du genou avec rupture du LCA ?
Le plus souvent, il s’agit d’une torsion du genou lors d’une réception d’un saut ou lors d’un changement de direction brutal, le pied restant bloqué au sol.
Parfois, il s’agit d’un mouvement de rotation interne pur du genou pied fixé au sol ou d’hyperextension (shoot dans le vide) qui entraîne alors généralement une rupture isolée du LCA.
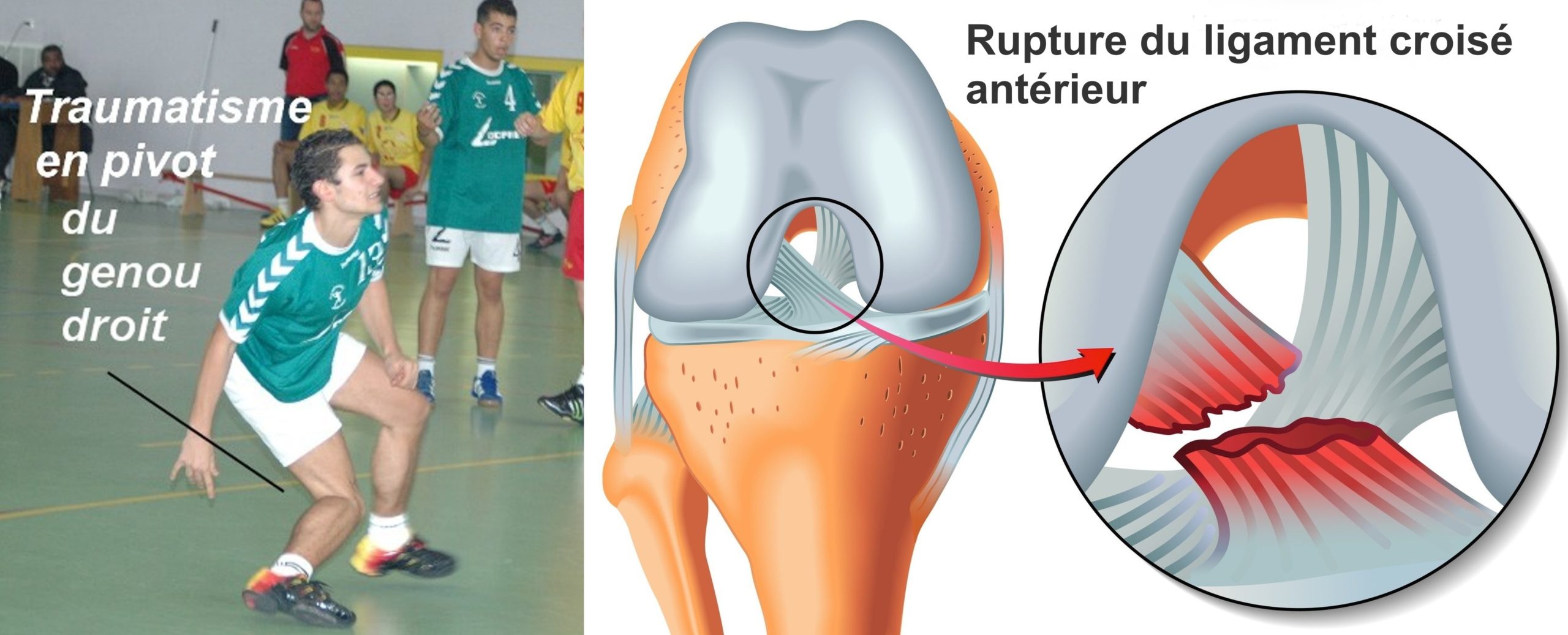
Comment se présente le genou ?
On recherche les sensations et les perceptions éprouvées par le patient lors du traumatisme :
Généralement impression d’accident grave : douleur, craquement, gonflement immédiat du au saignement,impotence et instabilité immédiates voire blocage du genou à cause de la douleur ou plus rarement à cause d’un morceau de ménisque déchiré et coincé.
Parfois, tableau beaucoup moins « bruyant » et risque d’absence de diagnostic : il vaut donc mieux consulter un orthopédiste devant tout tableau d’entorse du genou.
Comment fait-on le diagnostic ?
Il faut savoir qu’une translation tibiale antérieure (du tibia sous le fémur) est possible physiologiquement (on parle de laxité « naturelle », correspondant au jeu normal de l’articulation). Cette translation est symétrique et varie entre 3 et 10 mm selon les individus. La différentielle droite-gauche est généralement inférieure à 2 mm.
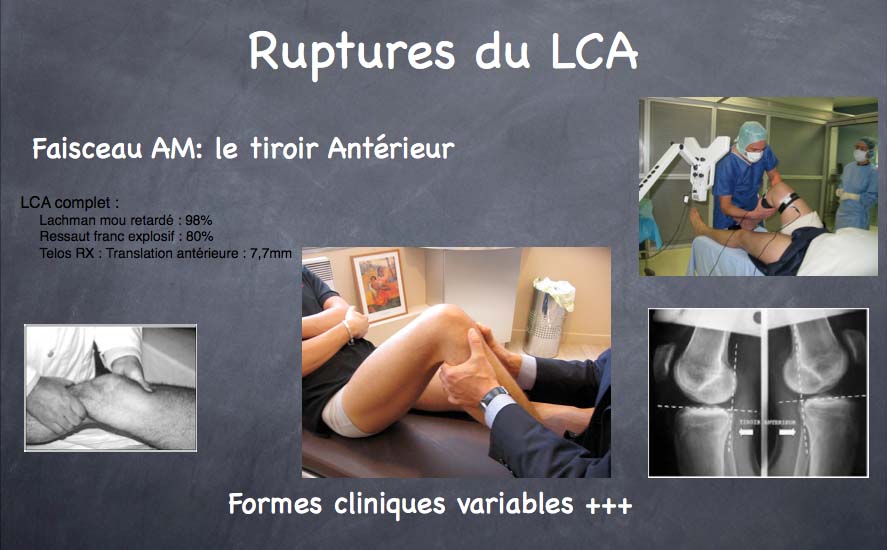
Si cette translation tibiale augmente, elle est l’expression d’une atteinte du LCA (élongation, rupture partielle ou le plus souvent rupture complète). L’évaluation de la laxité articulaire sera donc le temps essentiel de l’examen du genou.
Elle permet d’apprécier avec précision le degré d’atteinte des lésions ligamentaires (recherche d’un mouvement de tiroir, d’un ressaut rotatoire). Néanmoins, au stade aigu, la mise en évidence de ces tests cliniques est difficile chez les patients douloureux ou contractés.
Dans ces situations, les examens complémentaires seront d’une aide précieuse :
Les clichés du genou de face et de profil permettent d’éliminer une fracture. Ils peuvent être complétés par des examens dynamiques en mouvement de tiroir antérieur (TELOS), que l’on demande plutôt à distance de l’accident pour ne pas aggraver la douleur
Le scanner permet souvent de faire le diagnostic mais cet examen n’est pas le plus adapté pour étudier les parties « molles » (tissus, ligaments…). Le grand avantage est de pouvoir en bénéficier rapidement
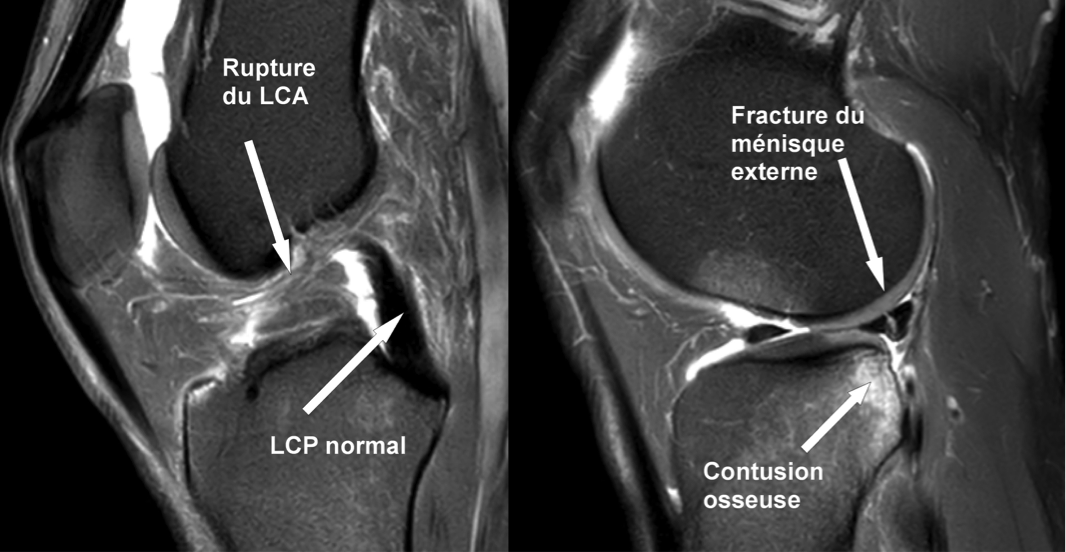
L’IRM est de plus en plus pratiquée mais les délais d’attente de l’examen sont très inégaux selon les régions. Il s’agit du meilleur examen d’imagerie pour poser le diagnostic mais il ne faut oublier qu’il s’agit d’un examen statique : comme pour le scanner, l’IRM ne peut apprécier la valeur fonctionnelle du ligament restant, rompu ou cicatrisé.
Seuls l’examen clinique et à un moindre degré les clichés radiographiques en stress (TELOS) peuvent donner ce type d’information
L’examen sous anesthésie générale, plus ou moins complété par un geste chirurgical d’emblée (arthroscopie pour vider un genou ou traiter une lésion du ménisque) ont longtemps été pratiqués : ils sont désormais désuets du fait de la qualité et de l’accessibilité des moyens d’imagerie modernes.
Seules les situations imprécises (genou inexaminable, suspicion d’atteinte multi-ligamentaire à l’imagerie) peuvent justifier ces gestes « agressifs ».
Quelles sont les conséquences d’une rupture du LCA ? Pourquoi l’instabilité qui en découle est dangereuse pour l’articulation ?
En cas d’entorse bénigne (entorse du LLI), l’évolution est le plus souvent favorable sur le plan de la stabilité, parfois moins sur le plan des douleurs résiduelles.
Par contre, dans les entorses graves comprenant une atteinte du LCA, l’évolution est souvent plus imprévisible
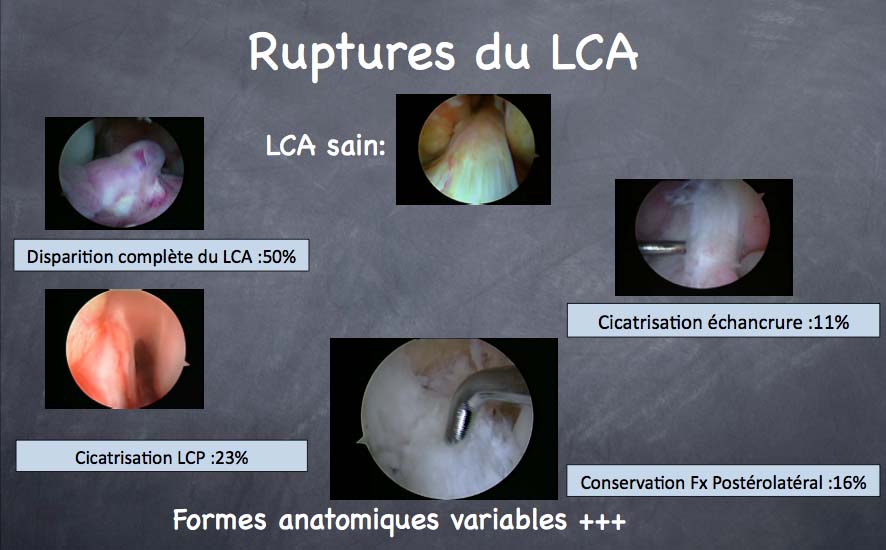
Soit le ligament « cicatrise » en se fixant sur l’autre ligament croisé (le LCP): on parle alors de « nourrice », une « bonne » nourrice pouvant limiter de manière satisfaisante la laxité anormale. Cette situation est fréquente passée la quarantaine, et permet de contrôler la laxité surtout si le patient est sédentaire et ne pratique pas de sports nécessitant des mouvements de pivot.
Soit la rupture du LCA entraîne une dégradation progressive de la stabilité du genou (au départ pour les sauts, les accélérations brutales ou les changements de direction rapides puis rapidement dans la vie de tous les jours). Dans ce cas de figure, cette laxité, pourvoyeuse d’épisodes aigus de dérobement est dangereuse pour l’articulation car elle est responsable de lésions méniscales par cisaillement, d’épanchements chroniques et de distension progressive des autres structures ligamentaires. Progressivement, ces phénomènes peuvent provoquer des lésions du cartilage articulaire aboutissant à la longue à une arthrose du genou.
Pourquoi traiter ? Quels sont les différents traitements proposés, qu’ils soient médicaux ou chirurgicaux ?
Traiter un genou victime d’une entorse grave permet d’espérer de limiter les séquelles qui sont représentés en premier lieu par l’instabilité de l’articulation (et ses conséquences néfastes à terme exposées plus haut), en second par la raideur.
Deux types de traitement existent. Ils sont souvent complémentaires :
Le traitement fonctionnel (la rééducation) a comme objectif final de palier à l’insuffisance ligamentaire par un renforcement musculaire, de façon à prévenir toute situation à risque pour le genou. Il mérite d’être tenté à chaque fois car il comporte de nombreux avantages (prévention des complications notamment de la raideur, rôle antalgique surtout dans les premières semaines, et bien sûr absence d’intervention chirurgicale).
Phase I : lutte contre les phénomènes inflammatoires : antalgiques, glaçage, immobilisation la plus courte possible dans une attelle pour éviter une sidération musculaire, ponction évacuatrice si besoin en cas de volumineuse hémarthrose, appui progressif.
Phase II : phase de rééducation proprement dite : récupération progressive des amplitudes, lutte contre la sidération du quadriceps et renforcement des muscles de la face postérieure de la cuisse (les ischio-jambiers), qui s’opposent naturellement au mouvement de tiroir antérieur.
Phase III : phase de travail proprioceptif : travail du contrôle musculaire du genou dans les situations à risque (récupération des sensations de l’appui) puis reprise sportive progressive en interdisant les mouvements de pivot.
INFORMATION CONCERNANT LES ENTORSES DU GENOU
Vous vous plaignez d’une douleur au genou qui a toutes les caractéristiques d’une entorse avec rupture du ligament croisé antérieur. D’autres formations peuvent être touchées comme le ligament latéral interne, le cartilage, un ménisque ou même l’os du tibia ou du fémur (contusion et saignement).
Ce problème est très fréquent, surtout chez les jeunes gens et le pronostic est fonction de l’âge (la cicatrisation en dépend), du type d’activités sportives pratiquées auparavant et des lésions associées.
Le ligament croisé antérieur est le principal stabilisateur du genou dans les mouvements en pivot (rotation autour de l’axe du membre inférieur). Il cicatrise peu ou mal et son atteinte va être responsable de deux types de mouvements anormaux : le tiroir antérieur (laxité du tibia en avant du fémur) et surtout le ressaut rotatoire (brusque avancée du tibia sous le fémur, vécu comme un déboîtement du genou). La philosophie du traitement est simple : retrouver une articulation indolore, mobile et stable de façon à éviter les lésions secondaires potentielles (ménisques, cartilages), conséquence de cette laxité anormale. A long terme, le but est d’éviter l’arthrose. Dans tous les cas, le traitement est d’abord médical, comprenant des antalgiques, une genouillère, des moyens physiques pour faire dégonfler l’articulation et une rééducation adaptée à la douleur.
Le but est la recherche progressive de la stabilité par les muscles environnants, de façon à pallier l’insuffisance ligamentaire. Il s’agit d’un travail s’étalant sur 6 semaines environ, à effectuer même si un geste de reconstruction du LCA est d’emblée envisagé.
Deux premières semaines :
Objectif : obtenir un genou peu douloureux et non inflammatoire
Moyens : aucun travail avec des poids pour ne pas aggraver l’inflammation, appui en fonction de la douleur, cryothérapie (glace) 3 à 4 fois par jour, mobilisation passive manuelle ou sur attelle motorisée (arthromoteur) de manière à prévenir la raideur et éviter le flessum (perte de l’extension), réveil du quadriceps (contractions isométriques -contraction de cuisse sans déplacement du genou-, electro-stimulation), lutte contre la fonte musculaire (amyotrophie) en faisant travailler les fessiers et les ischio-jambiers.
De la deuxième à la quatrième semaine :
Objectif : retrouver une marche et une vie sédentaire normale. Début de la « vraie » rééducation Moyens : toujours aucun travail avec des poids pour ne pas faire gonfler le genou, optimisation de la récupération des amplitudes articulaires (maintien de l’extension, travail de la flexion), renforcement musculaire progressif du quadriceps avec travail statique contre résistance de façon à « verrouiller » le quadriceps et à envisager le sevrage progressif de l’attelle, début du travail dynamique du triceps et des ischio-jambiers, début d’activités plus « physiques » (marche en piscine ou sur tapis roulant, vélo d’appartement dès 110° de flexion).
A partir de la quatrième semaine :
Objectif : Envisager un retour progressif aux activités sportives en ligne puis en pivot si le genou est stable
Moyens : Récupération complète des amplitudes (extension et 135/140° d’extension soit talon/fesse) par un travail passif comme avant et actif, poursuite du renforcement musculaire du quadriceps avec travail en chaîne fermée et co-contractions quadriceps/ischio-jambiers et surtout début du travail proprioceptif (d’abord en décharge puis en charge sur plateau de Freeman).
A cette date, une consultation de contrôle est nécessaire pour juger de la stabilité obtenue et décider entre traitement conservateur (rééducation seule) et reconstruction chirurgicale du ligament, en s’aidant parfois d’examens radiologiques complémentaires (radios TELOS, IRM…). Il faut savoir qu’aucune de ces méthodes ne donne à coup sûr 100% de bons résultats et qu’il n’est pas simple de choisir.
Qui opérer et quand ? Comment ? Qu’est-ce qu’une ligamentoplastie du LCA ?
Le traitement chirurgical permet d’espérer un LCA fonctionnel. Il s’agit d’un traitement radical souvent accompagné d’un très bon résultat clinique (stabilité, sports…), d’autant que la technique chirurgicale s’est affinée (gestes mini-invasifs, matériels résorbables, etc….). Néanmoins, comme pour toute intervention, il existe des risques à prendre en compte (cf infra). Il faut aussi se souvenir que la rééducation est souvent plus longue qu’avec le traitement fonctionnel (cf infra).
En fonction des particularités propres à chaque patient, (âge, activité sportive, type de sport, motivation), un traitement chirurgical pourra être proposé :
La suture en urgence du LCA rompu a été abandonnée en raison du taux d’échec important : on opte donc pour une reconstruction ligamentaire par une plastie du LCA
Cette reconstruction utilise donc une greffe, pour aboutir à la réalisation d’une « ligamentoplastie ».
Dans le même temps il faut traiter les éventuelles lésions des ménisques, conséquence de la laxité anormale du genou induite par la rupture du LCA

Fig 3 : Conséquences méniscales et traitement : méniscectomie partielle, suture méniscale
Les greffes artificielles (Gore-tex, Dacron), utilisées couramment il y a quelques années sont désormais abandonnées (rupture en fatigue à la longue, réactions immunitaires) tandis que les allogreffes sont interdites en France dans ce type d’indications. On utilise donc une autogreffe (ce qui a avantage l’emploi d’une structure vivante et comme inconvénient son prélèvement sur le corps humain).
Ce traitement chirurgical est légitime chez les patients jeunes pratiquant un sport de pivot ou de contact, chez les patients ayant une activité à risque (port de charges lourdes, travail en hauteur) ou chez les patients présentant des atteintes ligamentaires associées. Il est discutable dans les autres cas (pratique d’un sport sans pivot, genou déjà « fatigué », patient plus âgé) où le traitement est plutôt conservateur. Néanmoins, aucun patient n’est « abandonné » sous prétexte qu’il a dépassé 35 ans : certains ne sont pas instables à 25 ans (exemple : sédentaire non sportif), d’autres le sont à 60…
Dans tous les cas de figures, la rééducation est fondamentale et doit souvent être prolongée jusqu’à six mois voire un an. Le délai d’intervention est assez variable mais on n’opère plus le lendemain de l’accident comme il y a quelques années : il vaut mieux que le genou « refroidisse » et soit déjà rééduqué. Par ailleurs, en cas de « contusion osseuse » signalée à l’IRM, une intervention trop précoce risque de se solder par des suites difficiles (raideur +++)
En pratique, 3 situations sont rencontrées :
Patient très jeune (moins de 25 ans) et /ou exigence sportive importante (dans ces conditions, 90 % des patients ne peuvent reprendre leur sport au même niveau): intervention systématique, programmée dès le diagnostic fait, à distance suffisante de l’accident (quelques semaines)
Patient plus âgé, restant instable malgré une rééducation bien conduite ou n’acceptant pas de restreindre ses activités sportives : intervention proposée si patient motivé, plusieurs mois après l’accident initial
Patient ayant bien répondu à la rééducation (absence de dérobement, pas de sentiment d’insécurité), qui présente bien à distance de son traumatisme initial un accident aigu d’instabilité responsable d’une lésion méniscale (grosse déchirure), principe de l’intervention encouragé pour stabiliser ce genou trop laxe qui va mal évoluer. On tentera dans le même temps de réinsérer le ménisque ou au moins d’être économe sur la méniscectomie si celle-ci est nécessaire
Quelles sont les différents types d’intervention ?
Plusieurs techniques de reconstruction existent. Elles diffèrent par :
Le mode opératoire (chirurgie conventionnelle ou geste sous contrôle arthroscopique ,
actuellement considérée comme l’approche de référence: les gestes sont réalisés à l’aide d’une caméra miniaturisée dont l’image est retransmise sur un écran de télévision. Cette technique évite une grande ouverture de l’articulation, elle est par conséquent peu agressive)
Les différentes possibilités de réalisation des ancrages dans le tibia et le fémur (les tunnels)
Les différents moyens de fixation dans ces tunnels (vis, agrafes, attaches transfixiantes, …)
Surtout les différents types de greffe.
Ainsi :
Le greffon peut être prélevé au niveau du tendon rotulien (intervention de Kenneth-Jones, utilisant le 1/3 moyen du tendon avec une pastille osseuse prise en continuité du tendon de part et d’autre)
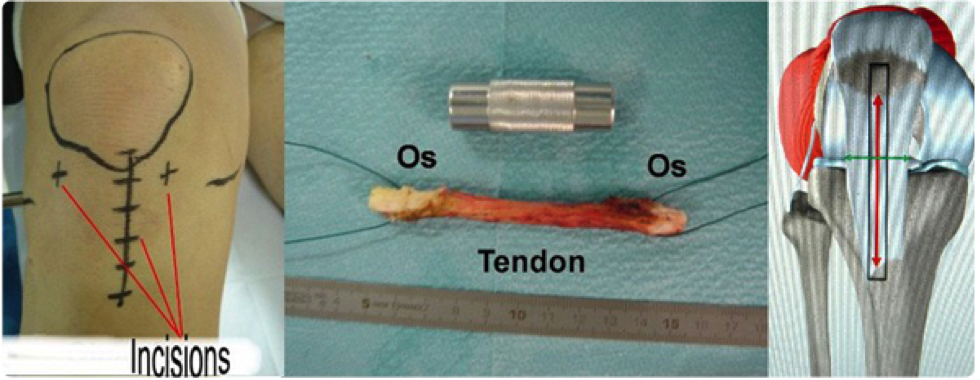
Avantages :
- Technique de référence
- Fixation solide (os contre os) autorisant une rééducation précoce
Inconvénients :
- Affaiblissement de l’appareil
- Risque de douleurs antérieures prolongées (1 an) Cicatrice médiane de 6/8 cm
Le greffon peut être prélevé au niveau des muscles ischio-jambiers (technique DIDT, c’est à dire Droit Interne/ Demi Tendineux):
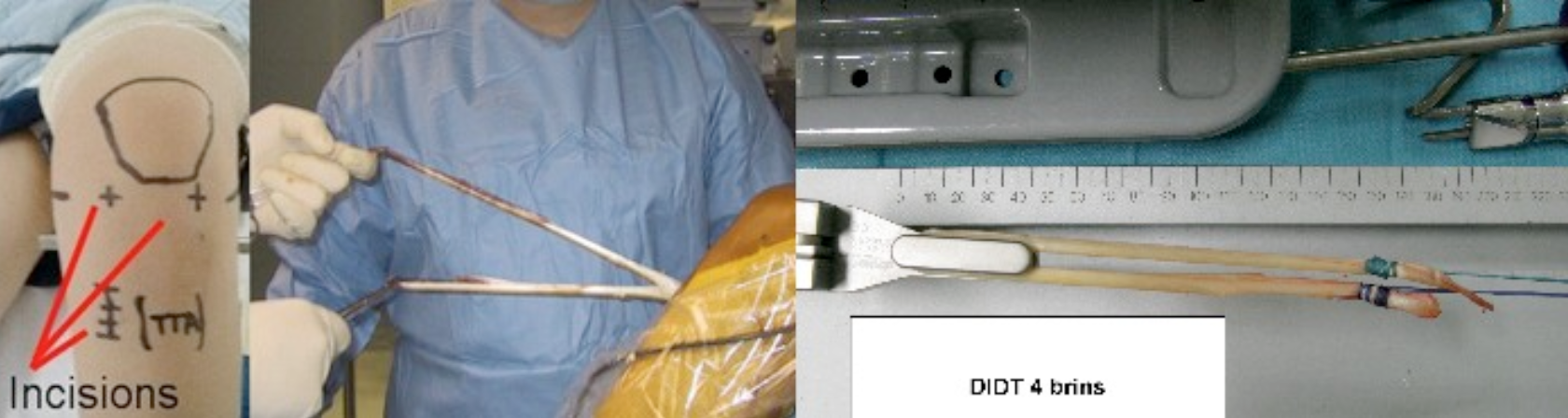
Avantages :
- Suites opératoires plus simples rendant plus facile la rééducation
- Cicatrice interne minime (2 cm)
Inconvénients :
- Lenteur de la fixation définitive dans l’os
- Solidité théorique moindre
- Risque de modification des tunnels (ballonisation)
- Prélèvement et donc affaiblissement des ischio-jambiers (muscles luttant contre le mouvement de tiroir antérieur)
Le greffon peut être prélevé au niveau des muscles ischio-jambiers mais ne comporter que la prise d’un tendon et non des deux. Dans ce cas, la greffe, pour avoir le même calibre est nécessairement plus courte mais sa longueur sera augmentée par la mise en place de bandelettes qui elles même seront vissées (technique DT4, c’est à dire Droit Interne replié en 4) :
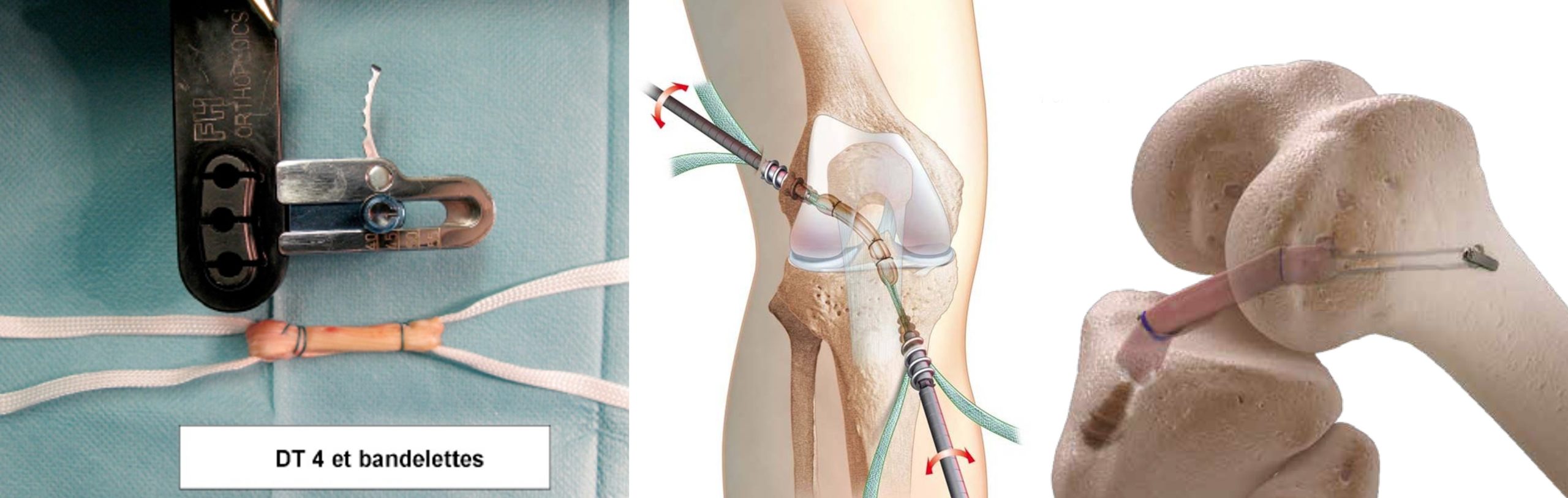
Avantages :
- Suites opératoires plus simples rendant plus facile la rééducation Cicatrice interne minime (2 cm)
- Affaiblissement moindre des ischio-jambiers
Greffes de gros calibres
Inconvénients :
- Utilisation d’une interface non vivante (bandelettes)
- Recul moins important (10 ans)
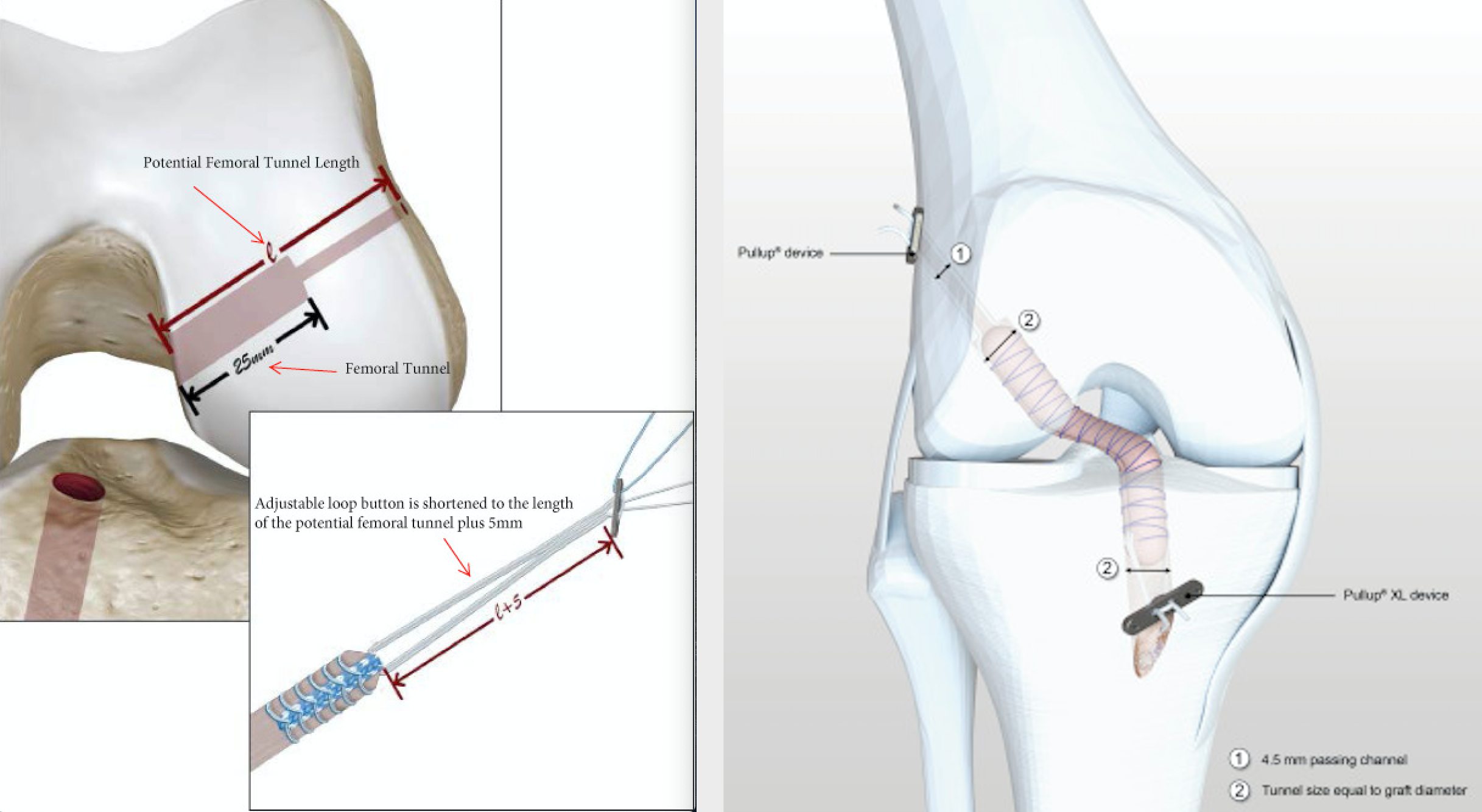
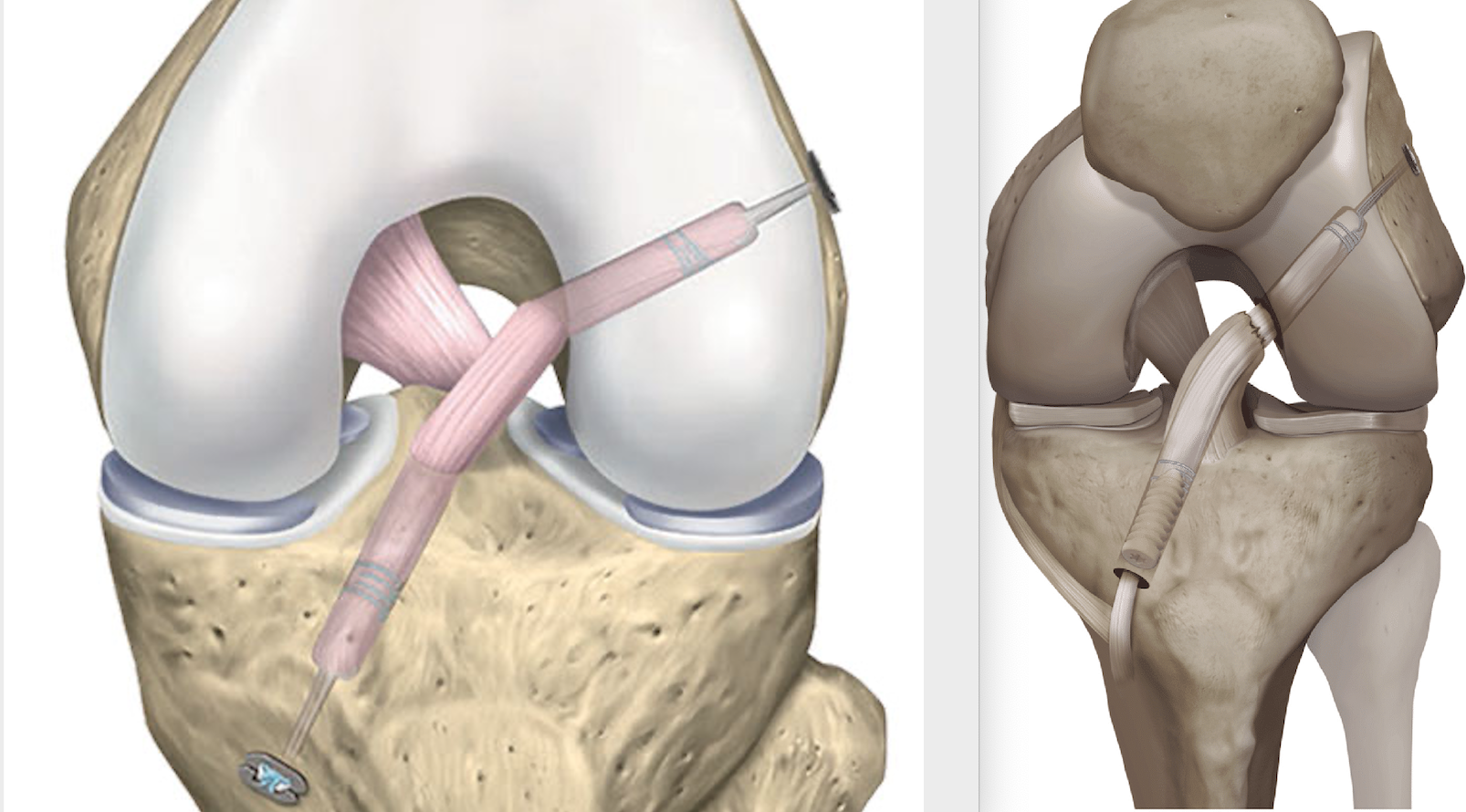
Le greffon peut être prélevé au niveau de la face externe de la cuisse (intervention de Mac Intosh au Fascia-Lata)
Avantages :
- Geste intra et extra- articulaire (effet ténodèse externe)
Plastie « dynamique » dans les 30 premiers degrés de flexion du genou
Inconvénients :
- Greffe à priori moins solide qu’un LCA normal
- Grandes incisions (15 cm minimum en externe, 5/6 cm en antéro-interne)
- Contrôle moins précis du positionnent de la greffe dans le fémur
- Suites opératoires plus longues (œdème prolongé en raison des décollementsmusculaires)
Dans certaines situations, ce type de greffe peut être utilisé en complément d’une technique intra- articulaire (Kenneth-Jones ou DIDT) : Il s’agit en fait d’effectuer une plastie anti-ressaut complémentaire (« retour externe »). Initialement utilisée seule (Intervention de Lemaire), cette plastie « protège » la reconstruction du LCA au prix d’un geste supplémentaire. On ne la préconise donc qu’en cas difficile à résoudre : échec d’une reconstruction du LCA (reprise chirurgicale), ressaut « explosif » à l’examen préopératoire, sportif pratiquant des activités en « pivot-contact ». Cette intervention complémentaire suscite un regain d’intérêt depuis quelques années car elle protège la ligamentoplastie en renforçant des structures existantes étirées ou rompues (voir plus loin).
Fig 8 : Ligamentoplastie sous contrôle arthroscopique (chirurgie vidéo-assistée)
Comment va se dérouler l’intervention proposée ?
Avant l’intervention
- Consultation avec le chirurgien. Explications de la technique proposée
- Délivrance des ordonnances (matériel à ramener, antalgiques)
- Consultation avec l’anesthésiste
- Arrivée à la clinique la veille de l’intervention ou le matin même
- Dernières recommandations (chirurgien/anesthésiste)
- Prise de médicaments le matin et/ou la veille de l’intervention (sédation légère)
- Ne plus manger 6 heures avant l’opération. Boissons gazeuses interdites 3 heures avant
Pendant l’intervention
- Douche obligatoire avec le savon-désinfectant approprié (une heure avant le départ vers le bloc)
- Arrivée au bloc opératoire (le brancardier vient vous chercher dans la chambre)
- Réalisation de l’anesthésie (anesthésie générale ou locorégionale type péridurale, souventcomplétée par une anesthésie du membre (« bloc périphérique »)
- Installation sur la table opératoire
- Mise en place du garrot pneumatique, de façon à éviter le saignement,
- Examen du genou « sous toutes les coutures », car vous ne sentez plus rien
- Mise en place des champs opératoires stériles
- Prélèvement de la greffe
- Réalisation de l’arthroscopie
- Nettoyage du reliquat de LCA, réparation éventuelle des ménisques.
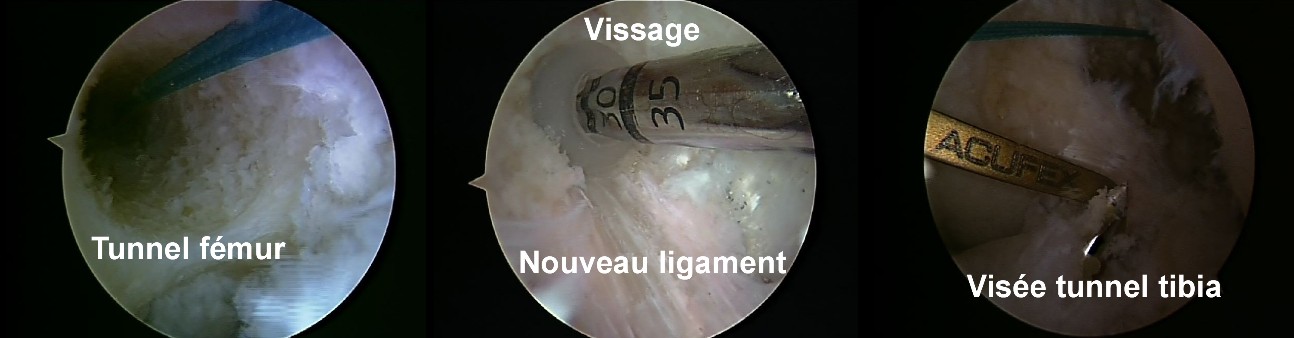
- Réalisation des tunnels dans le fémur et dans le tibia, grâce à un système de visée spécialPassage, tension et fixation de la greffe
- Fermeture après mise en place d’un drain chargé de recueillir le saignement post-opératoire
- Mise en place du pansement et de l’attelle réfrigérée
Après l’intervention
- Transfert vers la salle de réveil
- Contrôle de la douleur
- Vous regagner votre chambre ! (Le passage du brancard vers le lit peut s’avérer délicat, penserà la poignée surélevée pour vous aider !)
- Ne pas hésiter à appeler l’infirmière si la douleur monte pendant la nuit.
- Sortie possible le lendemain, parfois le jour même
- Maintien de l’immobilisation (3 semaines le plus souvent)
- Appui complet immédiat ou soulagé pendant 3 semaines selon les cas
- Antalgiques (antidouleurs) : utiles surtout les 10 premiers jours, surtout la nuit.
- Consignes précises de rééducation (cf infra)
- Cannes béquille 4 à 6 semaines
- Arrêt de travail (compter un minimum de 15 jours, même si activité sédentaire)
Quels sont les bénéfices que l’on peut attendre de cette intervention ? Quels sont les résultats ?
Cette intervention a pour but d’améliorer la fonction du genou en reconstruisant un nouveau LCA. Le but ultime est de faire disparaître le mouvement de tiroir antérieur et les dérobements dans les mouvements de pivot (brusque « ressaut »).
S’agissant du ressaut, il est contrôlé par la ligamentoplastie dans quasiment tous les cas. Il existe parfois une « ébauche » de ressaut résiduel, surtout sur les genoux opérés tardivement, où le temps a fini par distendre les ligaments de manière globale
S’agissant du contrôle de la laxité antérieure, les résultats sont souvent moins brillants, avec statistiquement une réduction moyenne de seulement 2/3 de l’excédent de laxité dû à la rupture du LCA (ex : pour un tiroir de 5 mm au TELOS du côté sain et de 20 mm du côté cassé, on peut espérer après chirurgie un tiroir antérieur résiduel de 5 à 10 mm). Cela ne semble pas avoir de conséquences fonctionnelles néanmoins car globalement la reconstruction du LCA est une intervention sûre et efficace, bien codifiée même si elle est en perpétuelle évolution.
Quelles sont les complications les plus fréquentes ?
Comme pour toute intervention, un problème anesthésique est possible même s’il est devenu rarissime, de même que l’atteinte d’éléments « nobles » durant la mise en place de la greffe (blessure d’une grosse artère, d’un nerf, etc….)
Comme pour toute intervention sur le membre inférieur, des soucis immédiats sont possibles : parmi les plus fréquents, citons l’hématome…Dans de rares cas, une phlébite (caillot de sang dans une veine) peut apparaître malgré la protection apportée par les anticoagulants instaurés de manière systématique. Citons aussi l’infection, particulièrement redoutée et prévenue, le plus souvent superficielle mais parfois profonde, pouvant alors justifier une deuxième intervention et une antibiothérapie prolongée. Enfin de très rares cas, des problèmes techniques (de prélèvement et/ou de fixation de la greffe, de réalisation des tunnels, de visualisation, etc …) peuvent amener le chirurgien à modifier le geste opératoire initialement prévu.
D’autres complications potentielles plus tardives méritent d’être citées même si elles sont rares en pratique courante :
La raideur est la plus fréquente et justifie une rééducation sérieuse, patiente, soutenue. Dépistée à temps, une fois écartée une algodystrophie, elle peut rendre nécessaire de faire « craquer » les adhérences sous anesthésie (« mobilisation »). Plus tardivement, il faudra envisager une arthrolyse (libération chirurgicale de l’articulation).
Une algodystrophie peut s’installer de manière insidieuse (douleurs nocturnes puis troubles trophiques -sudation, rougeur, œdème, douleur- avant l’installation d’une raideur difficile à traiter). Réputée régressive sans séquelles en 1 à 2 ans, cette complication d’origine inconnue est le plus souvent responsable de troubles définitifs à minima : raideur douloureuse, troubles trophiques (peau cartonnée, insensible ou au contraire susceptible)
L’arthrose à long terme est assez imprévisible : le fait de ne pas opérer risque de provoquer de
l’arthrose tandis que l’intervention en elle-même est arthrogène… Les patients les plus susceptibles de dégrader leur genou sont certainement ceux présentant déjà avant l’intervention des signes d’arthrose.
Comment se passe la rééducation postopératoire ?
Le but d’une plastie ligamentaire du LCA est d’obtenir un genou indolore, stable, mobile et fort afin de retourner aux activités antérieures
Il s’agit d’un programme thérapeutique long nécessitant motivation, confiance, discipline
La première étape, chirurgicale, n’est pas, contrairement à l’idée reçue, la plus difficile
La seconde étape, de réadaptation postopératoire, est la plus importante.
Votre collaboration est capitale, elle est le garant d’une bonne récupération fonctionnelle
Les principes sont la récupération des amplitudes articulaires, le contrôle actif de la musculature,
la rééducation à la marche et la reprogrammation sportive.
Il est important que cette rééducation n’entraîne pas de douleur, ni pendant ni après la séance.
Elle ne doit pas non plus provoquer d’épanchement dans l’articulation. Si cela arrive mieux vaut suspendre quelques séances, mettre le genou au repos et le glacer.
Les différentes phases de cette récupération sont adaptées au statut fonctionnel de chaque
patient. Elles différent aussi suivant le type d’intervention effectuée :
-
- Phase 1 (séjour hospitalier) : physiothérapie antalgique, 1er lever avec le kinésithérapeute (2 cannes anglaises ou une seule canne du côté non opéré), lutte contre l’œdème, mobilisation de la rotule pour limiter les adhérences, récupération progressive des amplitudes sur arthro-moteur sans dépasser 90°, réveil et « verrouillage » du quadriceps, consignes de repos, de surélévation pluriquotidienne et de glaçage du membre. Attelle nuit et jour.
- Phase 2 (approximativement de la 2ème à la 4ème semaine) : soins locaux, maintien des amplitudes avec un soin particulier pour les exercices en extension de manière à prévenir le flessum, abandon progressif de l’attelle la nuit et des cannes (courtes distances uniquement). Travail des ischio-jambiers. Consultation nécessaire si la flexion ne dépasse pas 90° à J+30.
- Phase 3 (approximativement de la 4ème à la 6ème semaine) : poursuite de la récupération de la flexion (objectif 110/120° à 6/8 semaines), assouplissements/étirements (les tissus cicatriciels sont rigides à cette période), marches longues autorisées (avec cannes), home-trainer. Plus d’attelle la nuit.
- Phase 4 (approximativement de la 6ème semaine au 3ème mois) : travail proprioceptif, réadaptation à la vie quotidienne avec intensification des exercices (appuis latéraux sans pivot, escaliers en descente, accroupissements prolongés), réadaptation aux pratiques sportives autorisées à la fin du 3ème mois (exercices en ligne type footing sur terrain plat, natation et bicyclette).
- Phase 5 (approximativement du 3ème au 6ème mois) : poursuite du travail proprioceptif, intensification des exercices (sauts, exercices d’agilité, vélo à 80 % de la force maximale), intensification de la pratique sportive toujours sans pivot (footing, vélo, natation).
- Phase 6 (approximativement du 6ème au 12ème mois) : intensification des activités sportives en force et en durée, reprise progressive des activités en pivot après le 7ème mois, sauf dans les activités avec pivot-contact, pour lesquelles il est préférable d’attendre 9 mois.
La rééducation
Une ligamentoplastie du LCA a été réalisée, consistant en un remplacement du LCA par une greffe au tendon Demi Tendineux.
L’attelle est déverrouillée d’emblée afin de vous permettre de plier la jambe. La marche s’effectue à l’aide de deux cannes, mais vous êtes autorisé à poser le pied au sol.
L’attelle et les cannes sont uniquement là pour protéger votre genou d’une éventuelle chute le temps que le genou redevienne plus fonctionnel et moins sensible.
Le nouveau ligament passe par une phase de fragilité relative avant l’ancrage osseux définitif, d’où une rééducation prudente et progressive selon trois phases successives :
Phase 1 : J1 à J15
La fixation du transplant est assurée exclusivement par le matériel, sans ancrage naturel osseux. Pour commencer à réveiller la jambe, vous êtes autorisés à ouvrir l’attelle et commencer à plier le genou et faire des contractions de la cuisse quand vous êtes assis ou allongé.
Il est préférable de commencer la kiné entre le 2ème et le 4ème jour post-opératoire. Un rythme de kiné à raison de 3 séances par semaine est suffisant.
Les différents éléments du travail en rééducation sont :
- Éducation du patient au positionnement fréquent du membre en déclive et au glaçage répété du genou.
- Massage du membre opéré à visée circulatoire et de drainage.
- Récupération progressive de la flexion passive à 90° et de l’extension complète de préférence sur arthromoteur.
- Mobilisation manuelle passive de la patella.
- Électrothérapie excito-motrice non tétanisante du quadriceps et triceps sural.
- Travail statique intermittent du quadriceps sans charge.
Phase 2 : J15 à J90
La fixation du transplant est toujours assurée par le matériel, sans ancrage naturel osseux suffisant, avec une phase de fragilité relative de ligamentisation progressive du transplant à partir du deuxième mois.
En fonction de l’évolution de chacun, l’attelle et les cannes sont arrêtées progressivement entre la 2ème et la 3ème semaine, d’abord à l’intérieur, puis pour les sorties. L’objectif est d’obtenir en toute sécurité un sevrage total des cannes et de l’attelle à J21.
Mais attention, ne pas faire de grosses sorties ou de marches prolongées au début pour limiter les inflammations. Toute apparition de réactions douloureuses ou inflammatoires doit imposer un travail moins intensif.
Les différents éléments du travail en rééducation sont :
- Poursuite du travail antalgique, circulatoire et anti-inflammatoire par les techniques de drainage et la cryothérapie systématique.
- Mobilisation manuelle passive de la patella.
- Électrothérapie excito-motrice des différents groupes musculaires.
- Poursuite du travail articulaire passif en flexion à 90° jusqu’à J30 puis récupération progressive indolore de l’intégralité des amplitudes.
- Travail statique intermittent du quadriceps avec charge proximale.
- Début du travail quadricipital en chaîne fermée à 1 mois, puis progressivement en chaîne ouverte.
- Travail des ischio-jambiers en mode d’abord statique à 90° de flexion puis dynamique.
- Début du travail proprioceptif d’abord en chaine ouverte puis progressivement fermée.
- Vélo et natation dans l’axe sans palme à partir du deuxième mois post-opératoire.
Phase 3 : après J90
L’ancrage du transplant est alors effectif.
Les différents éléments du travail en rééducation sont :
- Récupération complète passive et active des différentes amplitudes articulaires.
- Travail statique intermittent du quadriceps avec charge proximale.
- Travail quadricipital en chaîne fermée et en chaîne ouverte.
- Travail des ischio-jambiers en mode dynamique.
- Travail proprioceptif en chaîne fermée, progressivement adapté aux différentes contraintes professionnelles et sportives.
- Reprise de la course à pied d’abord dans l’axe et sur terrain stable puis réintégration progressive du geste professionnel ou sportif.
- Reprise d’activité sportive sans contrainte en pivot du genou au sixième mois post- opératoire.
- Reprise d’activité sportive avec contrainte en pivot du genou au septième mois post- opératoire.
- Reprise d’activité sportive avec contrainte en pivot et avec contact du genou au neuvième mois post-opératoire.
La rééducation devra être poursuivie jusqu’à une récupération complète et cessera avec le retour des habitudes antérieures de la vie quotidienne, professionnelle et sportive.
Quel est le devenir de la greffe ? Y a-t-il un risque d’échec ? Quelles sont les précautions pour l’éviter ?
La greffe, quand elle est prélevée, est détachée de ses artères nourricières : il s’agit d’un tissus devenu inerte qui à l’air libre finirait par se mortifier mais qui fixé dans le corps humain (ici le genou) va évoluer biologiquement avec le temps (nécrose progressive puis phase de nouvelle vascularisation à partir de l’os des tunnels). Cela va aboutir d’une part à une fixation solide et définitive et d’autre part à une modification des qualités mécanique de la greffe (de tendon, la greffe devient ligament). Cette « ligamentisation » prend de longs mois. Elle se poursuit en fait plusieurs années mais la seule conséquence importante à prendre en compte est la fragilisation de la greffe entre le 3ème et le 6ème mois post-opératoire. Durant cette période, il faudra donc être prudent (pas de sport en pivot avant 7 à 9 mois).
La reprise imprudente de sollicitations dangereuses pour le nouveau LCA est donc le premier risque d’échec. D’autres existent et en dehors d’une faute technique évidente (mauvaise indication ou taille de greffe, mauvaises positions de tunnels, fixations insuffisantes) sont le plus souvent imprévisibles. Ils concernent le devenir de la greffe (allongement, rupture, cicatrisation anarchique responsable d’une raideur en extension -syndrome du cyclope-) ou le devenir de sa fixation (faillite avant consolidation finale, modification ultérieure des tunnels à l’origine d’une faillite secondaire). Les progrès sont néanmoins constants, même si « refaire la nature » est une gageure….
Que faire en cas de rupture itérative ? (Échec d’une première intervention ?)
Il s’agit d’une situation de plus en plus souvent rencontrée puisque les reconstructions du LCA sont devenus plus courantes depuis une ou deux décennies, du fait à la fois de l’intensification des pratiques sportives et des connaissances actuelles concernant l’évolution néfaste à long terme d’un genou instable. Les échecs sont donc statistiquement plus nombreux (en valeur absolue car en pourcentage, les causes pourvoyeuses d’un échec ont fait l’objet d’études et sont connues pour la plupart).
La reconstruction chirurgicale itérative du ligament croisé antérieur reste donc indiquée pour les patients ayant une instabilité récurrente après échec d’une première ligamentoplastie. On s’en doute, la cause de cet échec doit être parfaitement analysée. Cependant parfois, aucune cause évidente n’est individualisée.
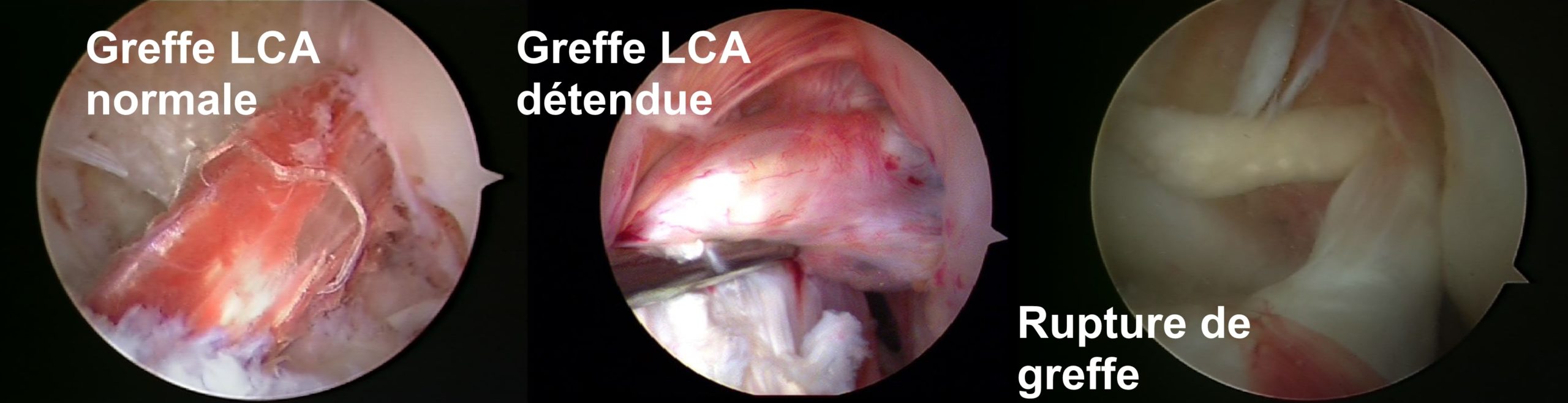
Fig 9 : Vues arthroscopiques d’une ligamentoplastie du LCA
Des choix doivent être faits et réfléchis. Ils concernent :
- Le choix de la nouvelle greffe (tendon rotulien, DIDT, fascia lata, ligament artificiel voire prise de greffe sur l’autre genou…)
- Le choix de la technique (arthroscopique ou à « ciel ouvert »)
- Le positionnement des tunnels effectués auparavant et leur état : peux-t-on les reprendre, faut-il les greffer, faut-il les changer d’endroit ?
- Le nouveau type de fixation de la greffe
- Le traitement d’autres laxités associées qui doivent être reconnues et corrigées pour obtenir un bon résultat
- La réalisation d’une plastie complémentaire externe anti-ressaut type Lemaire ou nouvelles plasties externes (voir plus loin)
Tout ceci rend compte des principales difficultés rencontrées dans les reconstructions itératives du ligament croisé antérieur. Les résultats de la chirurgie de reprise dans la reconstruction du LCA sont globalement moins bons que dans la chirurgie de première intention. Cependant, cette chirurgie semble très efficace pour une part très importante des patients (qui constituent en fait une population très hétérogène).
Néanmoins, les patients doivent être raisonnables dans leurs exigences et comprendre que le but principal de la chirurgie de reprise est plus de permettre un retour aux activités de la vie quotidienne que la reprise de la compétition sportive.
Les progrès depuis 20 ans
La chirurgie de reconstruction du ligament croisé antérieur est fréquente et désormais considérée comme mature et codifiée avec 85% de bons résultats fonctionnels et anatomiques. Néanmoins, il existe dans 15% des cas un ressaut présent et 10% de chirurgie itérative.
Surtout en dehors des erreurs techniques évidentes comme la malposition des tunnels, il est apparu que la cinématique post-opératoire était anormale, qu’elle soit antérieure ou surtout rotatoire.
Grâce à la navigation chirurgicale des cartes d’anisométrie favorable ont été établies (zone de positionnement préférentielle de la greffe) et d’autres auteurs ont établi de façon objective les rôles des différents faisceaux du ligament croisé antérieur.
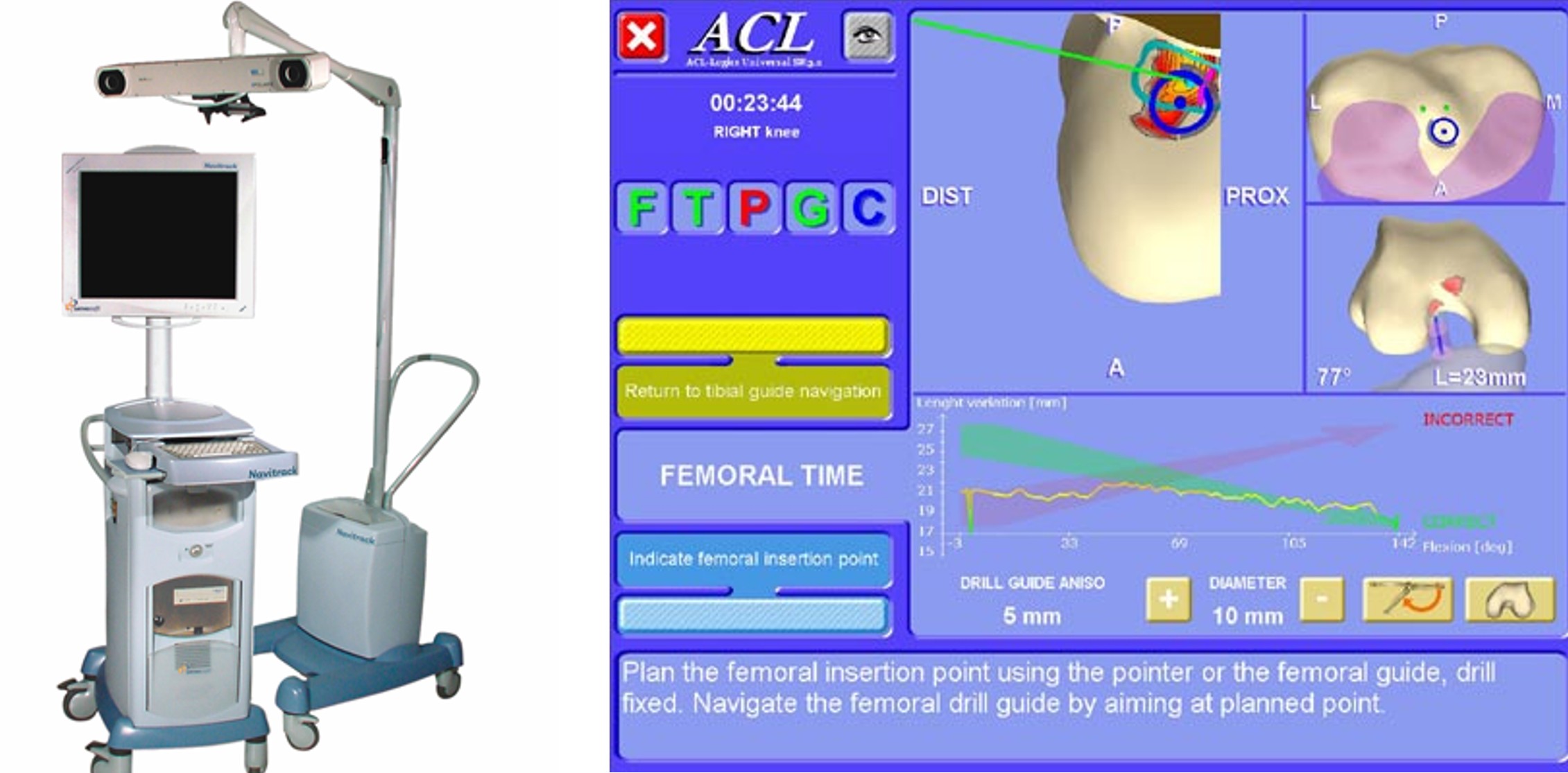
Fig 10 : Chirurgie assistée par ordinateur
Parallèlement la technique chirurgicale a évolué avec l’instauration des reconstructions à double faisceaux. Mais après un engouement mondial il y a 15 ans, cette évolution est désormais quasi abandonnée par tous.
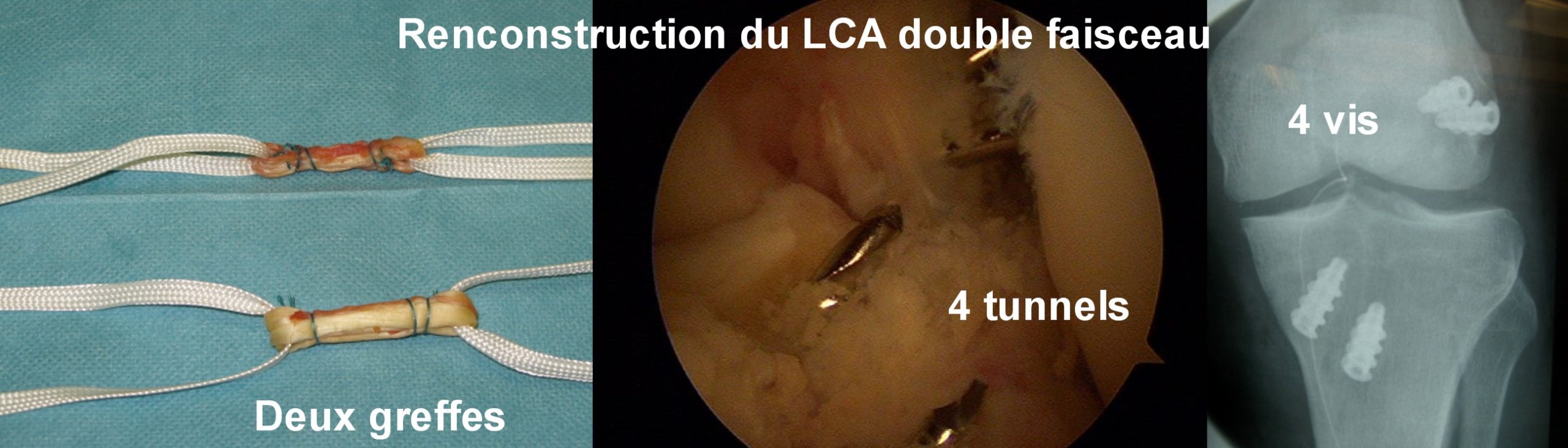
Fig 11 : Chirurgie du LCA, technique double faisceaux
Enfin de nouveaux outils d’évaluation ont été proposés visant par différents moyens à préciser l’analyse cinématique de ces genoux avant et après reconstruction du LCA.
Après s’être focalisé sur les mesures de la laxité antérieure facilement analysable par des radios, il est apparu qu’il fallait surtout mécaniser le ressaut rotatoire, mouvement complexe associant flexion, valgus et rotation interne dont dépend directement la satisfaction des patients mais dont la réalisation et l’analyse restent encore subjectives.
On s’oriente donc actuellement vers une analyse cinématique non invasive légère permettant des examens rapides que ce soit en consultation, au bloc, pour les deux genoux, à un coup raisonnable. C’est dans cette perspective que nous avons initié un projet en 2010 en partenariat avec l’Université Technologique de Compiègne.
Cette étude pilote toujours en cours évalue par un procédé tri dimensionnel non invasif comportant des capteurs inertiels incluant notamment des accéléromètres et des gyroscopes capables de mesurer des vitesses angulaires et de définir la vitesse de rotation instantanée du fémur autour de l’axe de rotation instantanée du tibia en fonction de la flexion. Les premiers résultats ont été présentés en Congrès national en 2013.

Quels sont les résultats ?
- C’est possible et c’est facile : 45 sec suffisent. C’est même possible en peropératoire, pansement fait, avant une éventuelle ténodèse externe associée
- Le recueil du signal est parasité par les mouvements des capteurs à l’interface peau/os, mais ceci gêne peu les accélérations et peut être minimisé
- Il n’existe qu’une reproductibilité intra-observateur car nous avons tous une façon différente de réaliser le ressaut rotatoire
- Nous avons pu quantifier l’amélioration du grade de ce ressaut entre le pré et le post-opératoire grâce à ce type de résultat :
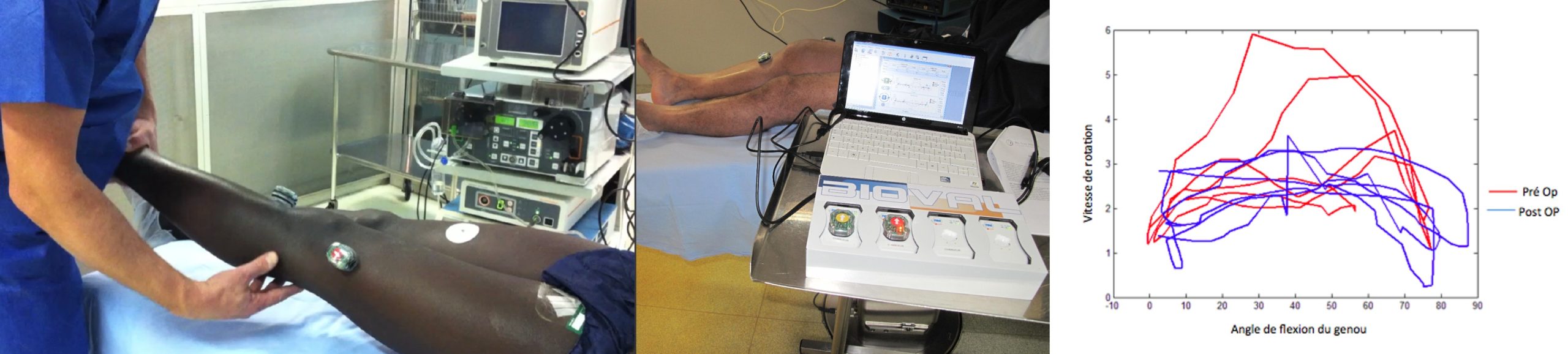
Fig 12 : Analyse cinématique non invasive pré et postopératoire
En rouge, la courbe préopératoire avec une vitesse de rotation instantanée qui culmine vers 30° lors de l’apparition du ressaut et diminue ensuite. La courbe en bleue montrant par contre en post-opératoire une vitesse instantanée de rotation quasi-identique quel que soit le degré de flexion du genou indiquant donc qu’il n’y a plus de ressaut et donc que le genou est désormais stabilisé.
A terme, l’utilisation de capteurs inertiels devrait offrir à terme la possibilité d’obtenir des mesures cinématiques objectives et personnalisées de façon non invasive à partir d’une acquisition rapide pratiquée en routine clinique. Ceci devrait permettre :
- En préopératoire, d’établir le classement des laxités en différents groupes.
- En postopératoire, de juger de ce que l’on a fait et de décrire la cinématique des patients insatisfaits qui est surement en rapport direct avec une insuffisance de correction de la laxité rotatoire même en cas de laxité sagittale réduite. Ces mesures permettent enfin d’espérer personnaliser la reconstruction du LCA et pourquoi pas d’aider à la décision ou à la réalisation de gestes complémentaires tel qu’un renfort externe.
Les avancées récentes : le retour des renforts externes (plasties extra-articulaires)
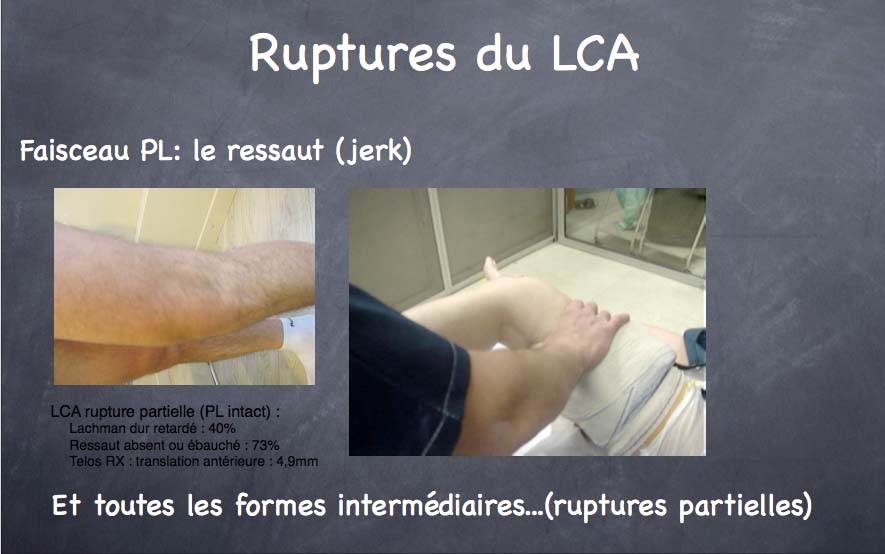
L’instabilité du genou qui résulte de la rupture du LCA est la conséquence d’une double laxité : à la fois sagittale (mouvement de tiroir antéro-postérieur) et rotatoire (subluxation antérieure du plateau tibial latéral en passant de l’extension à 30° de flexion (la réduction de ce mouvement définit le ressaut rotatoire ou Jerk Test).
Il faut savoir que lors de l’entorse du genou, le mécanisme en rotation n’a pas seulement cassé le ligament croisé antérieur qui se situe au centre du genou mais à créé également, dans des proportions variables, des lésions de la capsule antérolatérale (c’est à dire une distension variable des structures externes qui constituent les freins secondaires).

Fig 13 : Conséquences biomécaniques d’une rupture du LCA
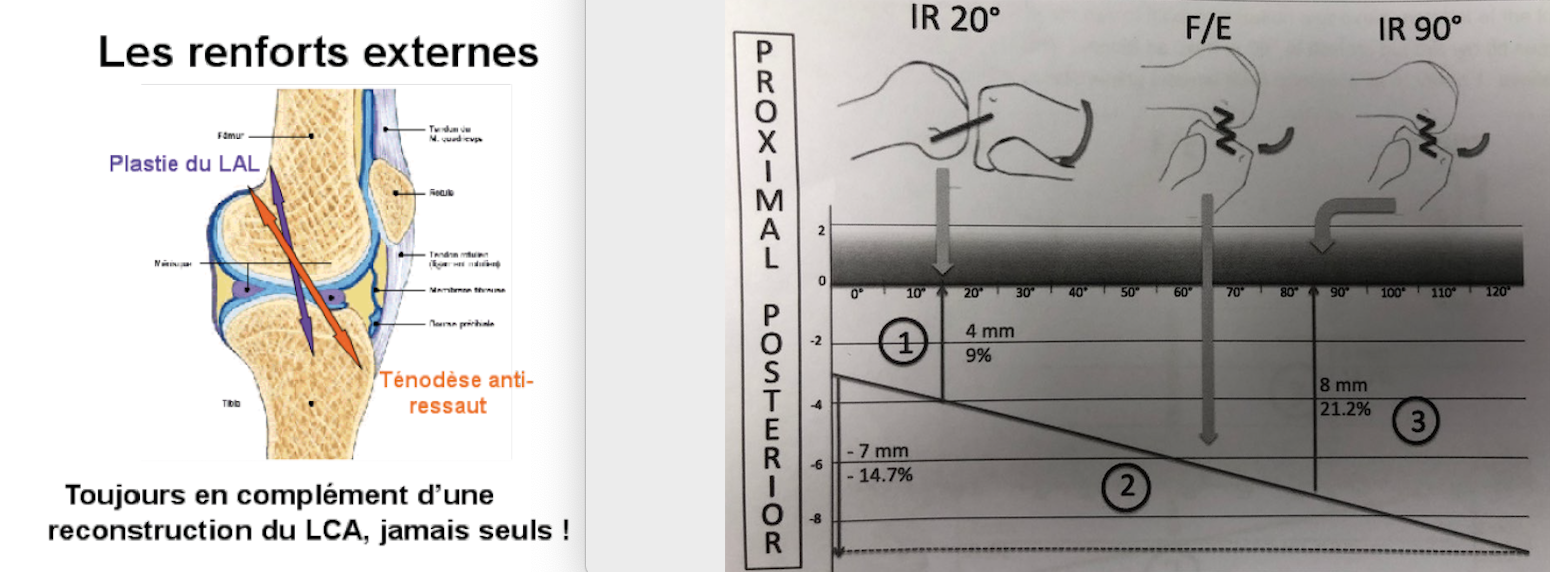
Initialement, dans les années 60, ce sont ces structures externes qui ont été renforcées avec des interventions créées pour palier aux conséquences de la rupture du ligament croisé antérieur qu’on ne savait pas remplacer alors. En France, Marcel Lemaire, en 1967, a décrit sa ténodèse anti-ressaut restée célèbre.
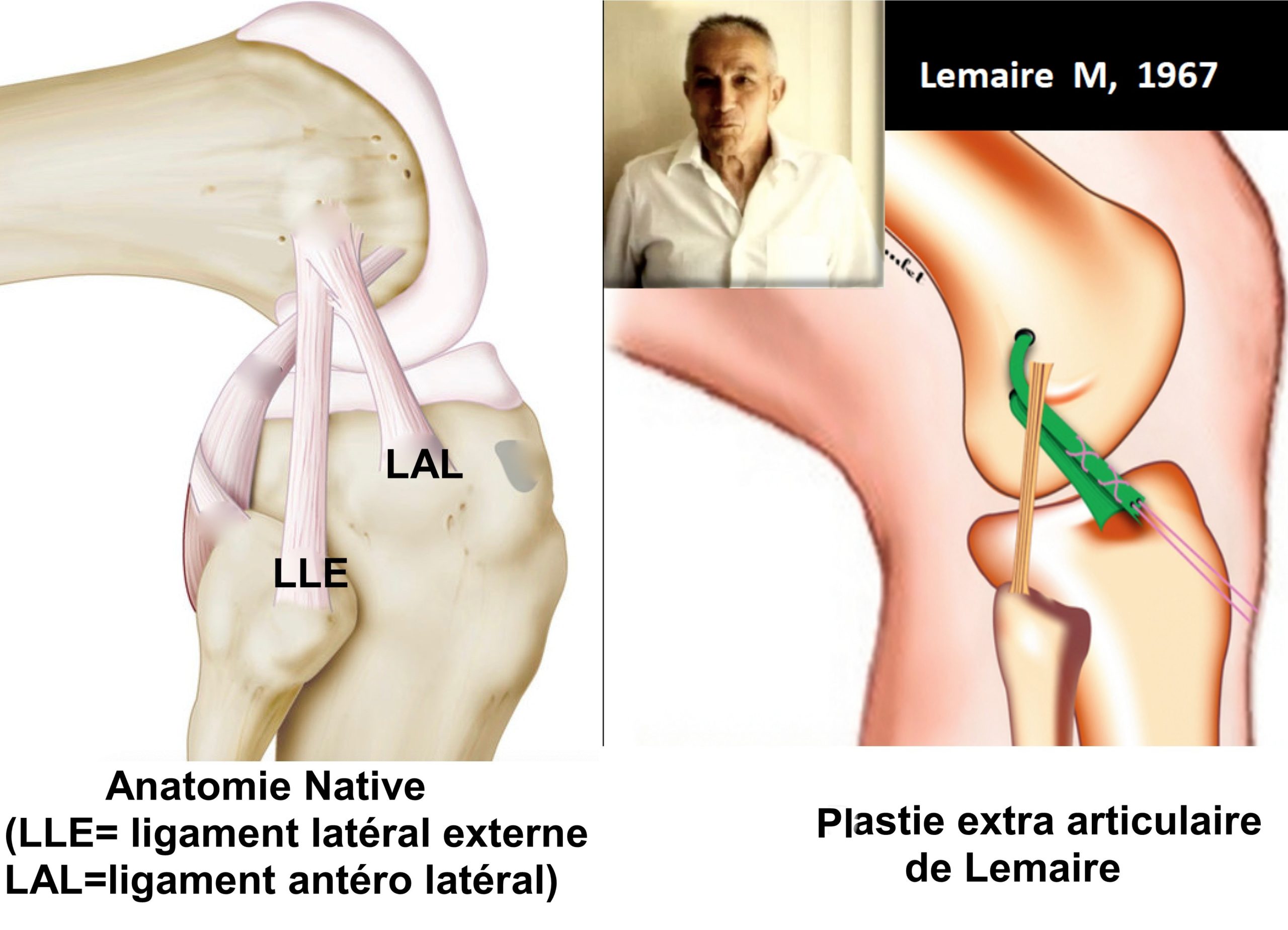
Fig 14 : Anatomie du plan externe et description de la ténodèse ilio tibiale
Pourtant, ces interventions ont été abandonnées comme seuls traitements des ruptures du ligament croisé antérieur car elles se sont soldées par des raideurs, des détentes, des récidives du ressaut, des lésions méniscales et par l’apparition d’une arthrose externe, conséquence du serrage excessif en rotation externe.
S’est donc développée une chirurgie de remplacement du LCA avec des améliorations successives (autogreffe remplaçant les ligaments synthétiques, réparation sous arthroscopie remplaçant les opérations conventionnelles à ciel ouvert, reconstruction anatomique des faisceaux antéro-médian et postéro-latéral et reconstruction mono-faisceau puis double- faisceau, greffe courte, endos bouton réglable etc…). Les progrès sont sans fin !
Néanmoins et malgré ces améliorations, les résultats cliniques ne sont pas à la hauteur dans tous les cas avec une laxité résiduelle restant présente chez 15% des patients opérés.
On assiste donc à un regain d’intérêt pour les renforts externes associés à une reconstruction intra-articulaire du LCA depuis les années 2010, d’autant qu’une équipe belge, en 2013, a mis en évidence la présence inconstante d’une structure fibreuse renforçant la capsule appelée « ligament antérolatéral » ou LAL.
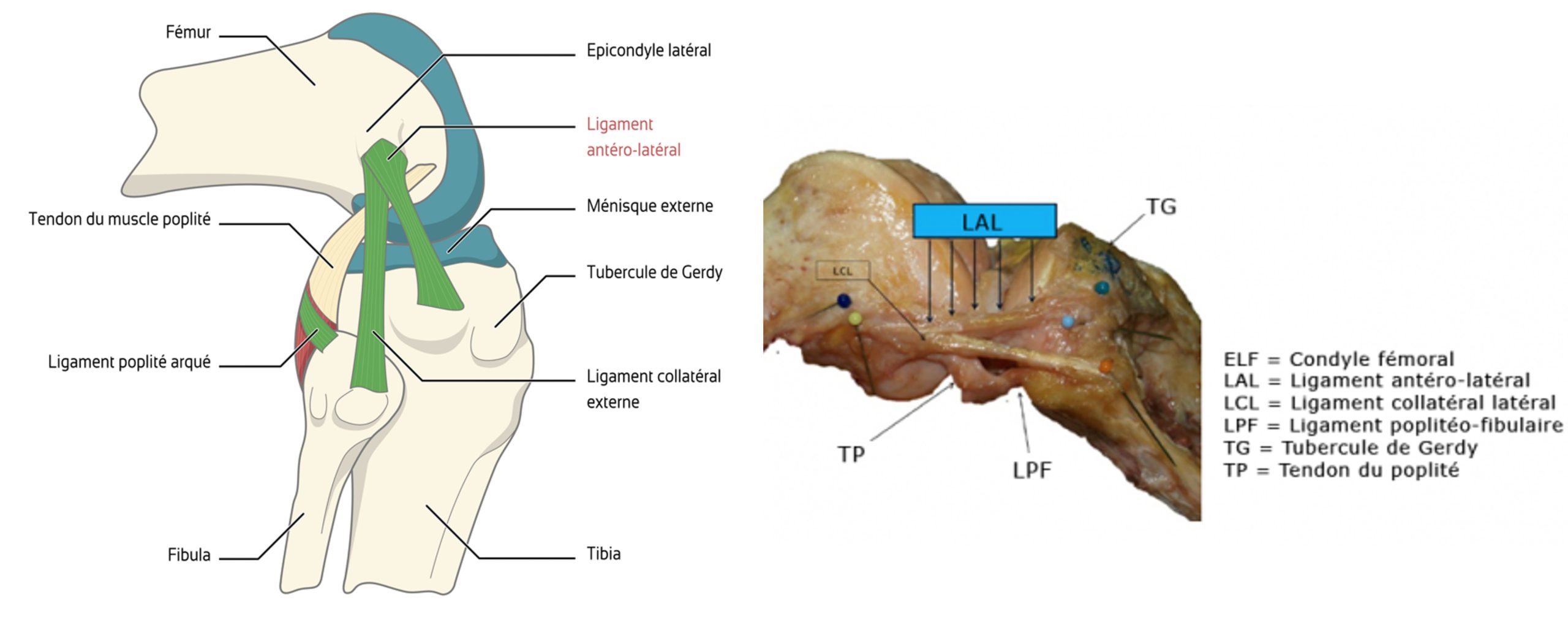
Fig 15 : Anatomie du plan externe et description du ligament antérolatéral
Depuis cette date, de nombreuses techniques ont été proposées : soit limitant le ressaut (ténodèse anti-ressaut), soit reconstruisant le ligament antérolatéral (plastie extra-articulaire).
Cette vision des choses est tout à fait logique en ce qui concerne le contrôle de la rotation interne excessive du plateau tibial latéral en reconstruisant le frein principal (ligament croisé antérieur) et les freins secondaires (formations tissulaires externes détendues et/ou cassées). Divers montages ont été proposés depuis une dizaine d’années avec des comportements biomécaniques malheureusement différents.
En effet, cette plastie doit être tendue à 30° de flexion mais détendue en extension complète, en flexion à 90 et surtout en rotation interne permettant ainsi la rotation interne automatique du genou.
Pour se faire, la greffe utilisée (qui ne peut être isométrique (longueur identique quelque soit l’angle de flexion du genou)) doit avoir une anisométrie favorable et donc des insertions anatomiques précises :
Du côté fémoral : l’origine de la greffe doit être située en arrière de l’épicondyle latéral et proximal par rapport à celui-ci,
Du côté tibial : l’insertion si situe à mi-chemin entre le tubercule de Gerdy et la tête du péroné (définie au mieux grâce à l’aide d’un compas afin d’avoir une isométrie en début de flexion).
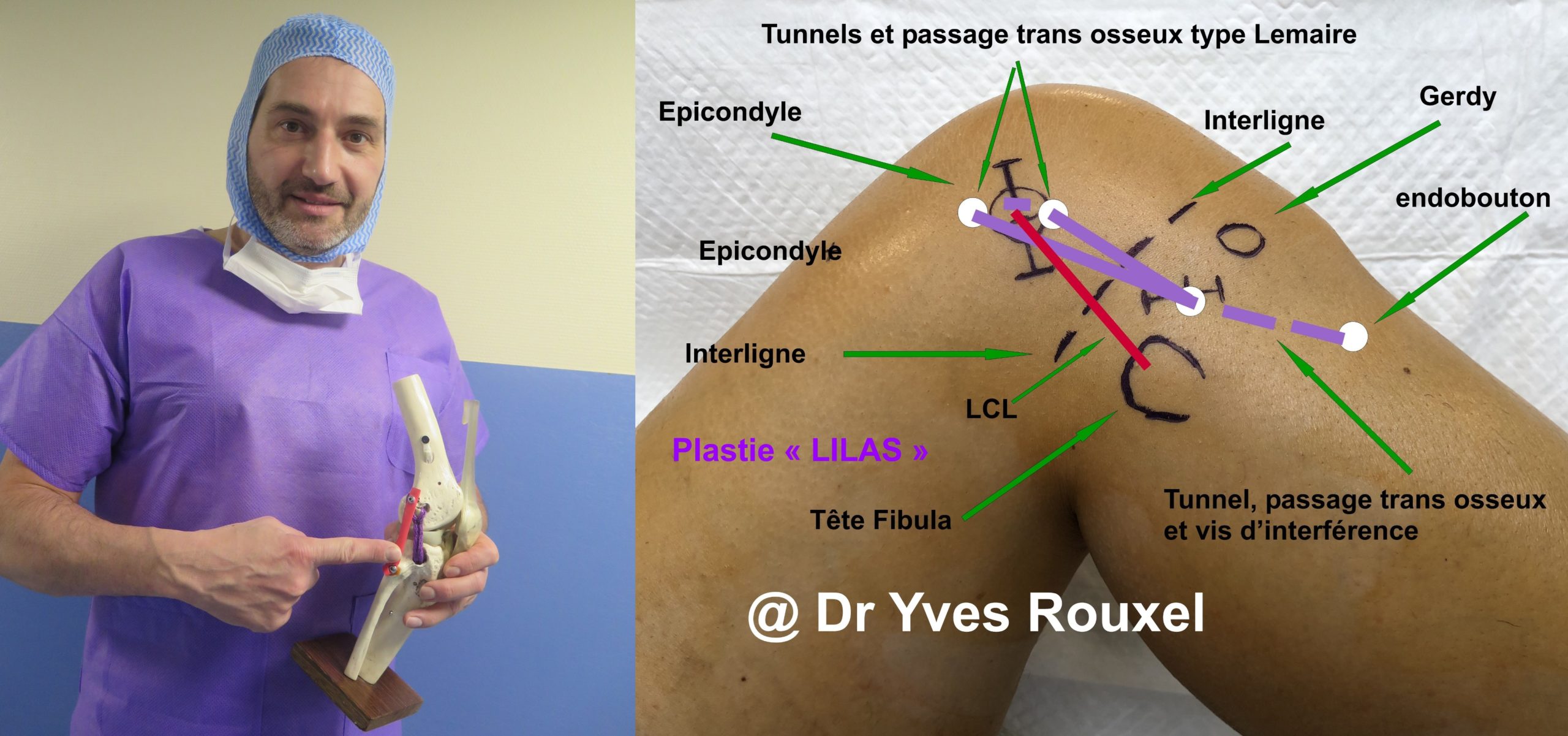
Fig 17 : Description de la plastie « Lilas », combinant ténodèse externe et reconstruction du LAL
Durant son trajet, cette plastie doit cheminer au mieux sous le ligament latéral externe afin d’éviter des variations excessives de longueur et de reproduire un effet poulie.
Partant de ces principes, notre équipe a mis au point une plastie inédite dénommée « Plastie Lilas » répondant au mieux aux divers prérequis trouvés dans la littérature.
Mise au point en 2018, elle requiert une grande habitude de la chirurgie du genou, à la fois arthroscopique et conventionnelle, et un réglage précis commun à toutes les ténodèses externes : serrage de la plastie à 20° de flexion en rotation neutre en évitant toute fixation en rotation externe excessive.
Les avantages espérés sont :
Une réduction significative du pourcentage de ressaut rotatoire résiduel,
Une répartition des contraintes avec une sollicitation moindre de la greffe du ligament croisé
antérieur et donc un moindre taux de rupture,
Une réduction des lésions méniscales et cartilagineuses secondaires
Les inconvénients sont :
Une intervention supplémentaire donc un temps opératoire plus élevé et des suites plus difficiles,
Une absence d’amélioration du tiroir antérieur résiduel ou des scores cliniques,
Une évaluation clinique difficile en l’absence de test mécanisable du ressaut rotatoire,
Un risque de dégradation cartilagineuse
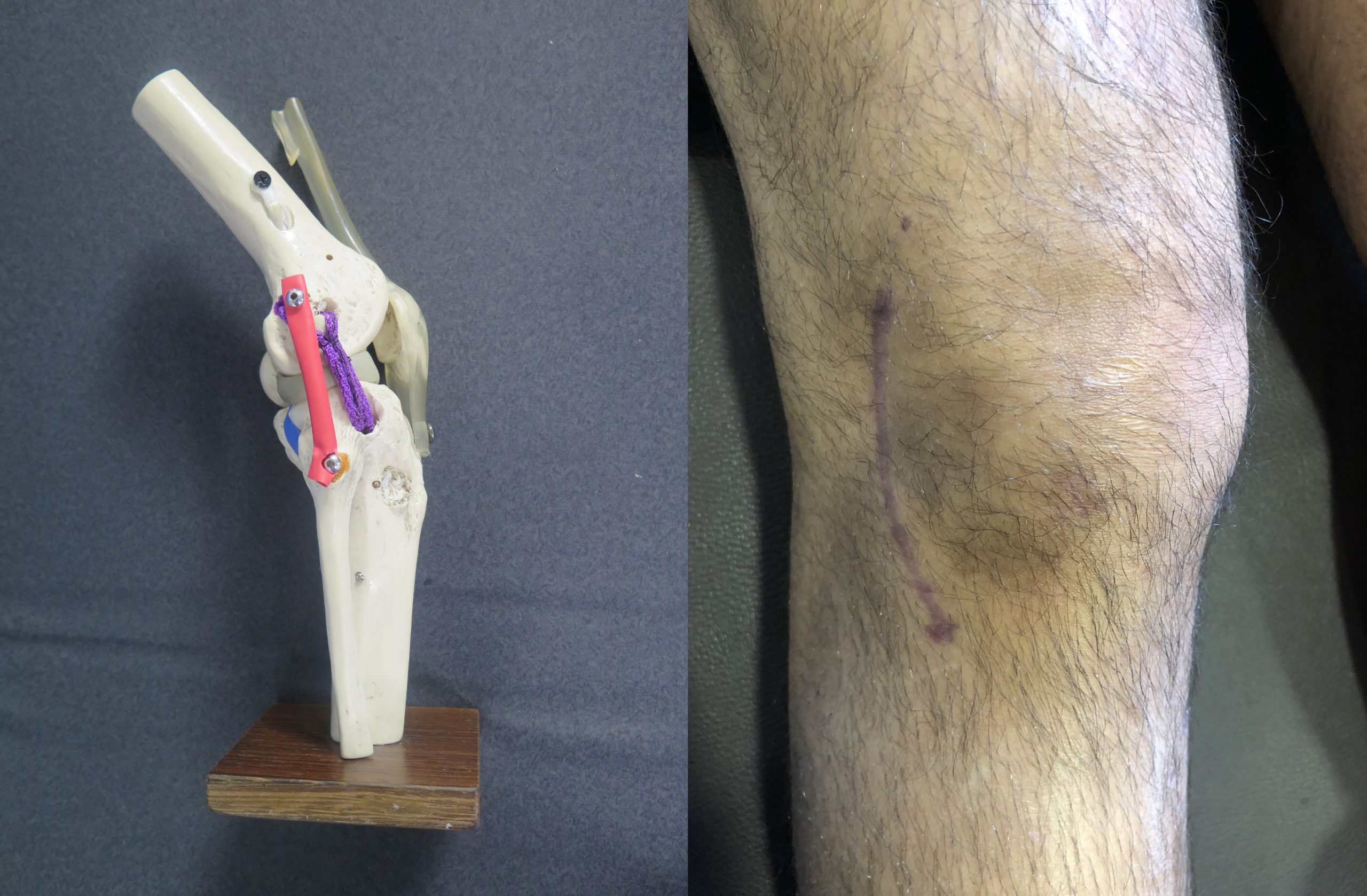
Fig 18 : Description de la plastie « Lilas » et aspect postopératoire
La situation actuelle (2020)
Un consensus d’experts existe définissant la place d’une plastie externe en complément d’une reconstruction du ligament croisé antérieur en cas de ressaut rotatoire explosif, sport de pivot- contact, sport professionnel, reprise de ligamentoplastie, hyperlaxité et recurvatum. Certains rajoutent les réparations méniscales chez le sujet jeune.

Cela permet de garantir au mieux le contrôle de la rotation interne ainsi que la protection de la plastie du LCA en évitant ainsi la récidive de rupture ou un accident de ménisque ultérieur.
Mais en 2020, en dehors de ces différentes évolutions techniques, l’heure est à l’évaluation objective de la cinématique du genou reconstruit quelle que soit la technique utilisée et c’est dans ce sens que nous travaillons depuis 2013.

On le voit, l’enjeu est la personnalisation du traitement en fonction du type de laxité présentée par le patient, ses prétentions sportives, les lésions associées des ménisques, l’état des cartilages et le type de greffe disponible pour reconstruire…







No Comments
Sorry, the comment form is closed at this time.